Широкая доступность антиретровирусной терапии значительно облегчила борьбу с ВИЧ. Но одних лекарств недостаточно. Нужно тщательно выбирать схему лечения и контролировать его в тесном сотрудничестве с лечащим врачом, поскольку как до, так и во время лечения могут возникнуть проблемы. Одной из наиболее важных из них является устойчивость ВИЧ к лекарствам.
К счастью, теперь мы много знаем о том, как снизить риск развития резистентности и лечить лекарственно-устойчивый вирус. Также в нашем распоряжении есть технологии, которые направлены на выявление лекарственно-устойчивых вирусов и которые помогают нам принимать решения в отношении лечения. Такое тестирование на лекарственную устойчивость стало обычной процедурой при лечении ВИЧ.
Что такое лекарственная устойчивость ВИЧ?
Говоря простым языком, лекарственная устойчивость обозначает способность болезнетворных микроорганизмов, таких как бактерии и вирусы, продолжать размножаться, несмотря на присутствие лекарств, которые должны их уничтожать.
В случае ВИЧ устойчивость к лекарствам вызывается изменениями (мутациями) в генетической структуре вируса. Эти мутации могут приводить к изменениям в некоторых белках, чаще всего ферментах, которые помогают ВИЧ воспроизводиться (реплицироваться).
ВИЧ мутирует очень легко и быстро. Это связано с тем, что ВИЧ реплицируется с чрезвычайно высокой скоростью и не содержит белков, которые обычно исправляют ошибки, совершаемые вирусом при копировании.
Мутации происходят случайно, ежедневно, но большинство из них безвредны. По сути, большинство мутаций фактически вредят ВИЧ — они снижают «приспособленность» вируса и замедляют его способность инфицировать клетки CD 4 в организме. Однако ряд мутаций помогает ВИЧ выживать даже при использовании препаратов против него, потому что эти мутации блокируют действие лекарств против ферментов ВИЧ, на которые они нацелены. Именно эти мутации имеются в виду, когда мы говорим о лекарственной устойчивости.
В процессе размножения ВИЧ внутри клетки человеческого организма участвуют несколько ферментов. Также к процессу подключаются белки, включая GP41, за счет которых вирус цепляется за клетки CD4 и инфицирует их. В любой из этих частей вируса могут происходить мутации, которые вызывают лекарственную устойчивость:
- Обратная транскриптаза: на этот фермент направлено действие нуклеозидных ингибиторов обратной транскриптазы (НИОТ) и ненуклеозидных ингибиторов обратной транскриптазы (ННИОТ).
- Интеграза: на этот фермент направлено действие ингибиторов интегразы.
- Протеаза: на этот фермент направлено действие ингибиторов протеазы.
- GP41: на этот белок, расположенный с внешней стороны оболочки ВИЧ, направлено действие ингибиторов слияния.
Для ВИЧ-инфицированных людей лекарственная устойчивость вируса означает, что лекарства становятся менее эффективными или даже полностью неэффективными, а это значительно сокращает варианты лечения.
Как это происходит?
Мутации резистентности ВИЧ к лекарствам могут возникать как до, так и во время лечения ВИЧ. Вот как это происходит:
- Передача лекарственно-устойчивого ВИЧ. Сейчас многие ВИЧ-положительные люди принимают лекарства от ВИЧ. Если у человека развилась устойчивость к одному или нескольким препаратам против ВИЧ и этот человек занимается незащищенным сексом или пользуется общими иглами с другими людьми, неинфицированными этим вирусом, то этот человек может заразить своих партнеров лекарственно-устойчивым штаммом ВИЧ, то есть таким вариантом вируса, у которого есть мутации, вызывающие резистентность. В Соединенных Штатах и других странах, где широко распространено лечение ВИЧ, от 5 до 20% людей впервые инфицируются штаммами вируса, устойчивыми по крайней мере к одному из препаратов от ВИЧ.
- При приеме препаратов предэкспозиционной профилактики (PrEP). В июле 2012 года «Трувада» (тенофовир плюс эмтрицитабин) была одобрена Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США для использования ВИЧ-отрицательными людьми, подверженными риску инфицирования этим вирусом. Люди, принимающие «Труваду» в качестве PrEP, подвержены потенциальному риску — если они инфицируются вирусом, но не сразу узнают об этом и продолжают принимать препарат, то у недавно приобретенного вируса может развиться устойчивость к одному или обоим действующим веществам, входящим в состав «Трувады». Стоит отметить, что в клинических испытаниях «Трувады» в качестве PrEP такое явление отмечалось очень редко. А если PrEP применяется в точном соответствии с инструкциями — ежедневно, независимо от того, запланирована или нет сексуальная активность, — эксперты считают, что риск развития резистентности крайне незначителен.
- Во время лечения. Даже если человек инфицирован ВИЧ, не содержащим мутаций резистентности («диким» вирусом), со временем с ним все равно происходят генетические изменения, даже до начала лечения. Это приводит к образованию в организме большого количества немного отличающихся друг от друга вирусов. Какие-то из них содержат мутации, которые могут частично или полностью противостоять антиретровирусным препаратам — именно поэтому в отношении ВИЧ никогда не применяется лечение одним препаратом (монотерапия). Вскоре после начала лечения комбинированными препаратами против ВИЧ количество вируса дикого типа резко снижается. Однако, если количество вируса не снижается и не удерживается на очень низком уровне, разновидности ВИЧ могут продолжать реплицироваться, приобретая дополнительные мутации. И как только вирус накопит достаточно мутаций, у него может развиться высокий уровень устойчивости к используемым лекарствам, что приведет к увеличению вирусной нагрузки и резкому снижению количества клеток CD4.
Основная проблема, связанная с этими мутациями, заключается в том, что они могут привести к перекрестной устойчивости. Это означает, что устойчивость ВИЧ к одному препарату может автоматически превратиться в устойчивость к другим препаратам того же класса. Например, если человек лечится по схеме, содержащей ННИОТ «Сустива», и вирус в его организме приобретает устойчивость к нему, то есть вероятность, что этот вирус будет также устойчив к воздействию ННИОТ «Вирамун» и «Рескриптор», даже если человек не принимал эти препараты.
Какие факторы способствуют возникновению резистентности во время лечения?
Если и существует одно «золотое правило» антиретровирусной терапии, то оно таково: чем ниже вирусная нагрузка во время лечения, тем меньше вероятность, что вирус продолжит размножаться и мутировать. Максимально действенная схема лечения ВИЧ — это наиболее эффективный способ поддерживать низкую вирусную нагрузку (желательно на неопределяемом уровне) и предотвращать появление новых мутаций.
К сожалению, существует ряд факторов, которые могут снизить эффективность схемы лечения ВИЧ, например следующие:
- Низкая приверженность лечению: чтобы лекарства от ВИЧ действовали в полную силу, их необходимо принимать в точном соответствии с предписаниями врача. Пропуск приема препаратов или неправильный прием лекарства может привести к снижению концентрации действующих веществ в крови. Если концентрация препарата становится слишком низкой, ВИЧ размножается более свободно и количество мутаций растет. Существует ряд причин, по которым людям бывает трудно строго соблюдать схему приема препаратов. Это могут быть побочные эффекты, напряженный ритм жизни или забывчивость. Если вам трудно соблюдать режим приема лекарств, не стоит этого стыдиться — лучше сообщите об этом своему врачу, чтобы он помог вам найти решения этой проблемы, в том числе, например, за счет упрощения схемы терапии.
- Плохая абсорбция (всасывание): препараты против ВИЧ нужно не только принимать строго по графику — они должны к тому же эффективно всасываться в кровоток. Если лекарство или комбинация лекарств должным образом не всасываются, то их концентрация в крови снижается, что в конечном итоге приводит к активному размножению ВИЧ и накоплению мутаций резистентности. Прием некоторых лекарств зависит от приема пищи, соответственно, несоблюдение этого требования может повлиять на абсорбцию препарата. Люди с ВИЧ также могут страдать от диареи и рвоты, из-за которых лекарства могут слишком быстро выводиться из кишечника и не успевать всасываться в кровь.
- Различная фармакокинетика: фармакокинетика — это научный термин, описывающий то, как лекарство всасывается, распределяется, расщепляется и выводится из организма. Взаимодействия между лекарствами, в том числе распространенными лекарствами от ВИЧ, может стать серьезной проблемой в этом отношении. Например, если НИОТ «Виреад» (тенофовир) скомбинировать с ингибитором протеазы «Реатаз» (атазанавир), концентрация «Реатаза» в крови может упасть до опасно низкого уровня. Вот почему при совместном приеме «Виреада» и «Реатаза» также нужно принимать ингибитор протеазы «Норвир» (ритонавир), который повышает концентрацию «Реатаза» в крови. Подобных взаимодействий между лекарствами довольно много. Обязательно сообщите врачу обо всех препаратах, которые вы принимаете, включая рецептурные и безрецептурные средства, а также витамины и пищевые добавки.
Как узнать о наличии лекарственной устойчивости у вируса?
Один из лучших и самых доступных способов проверить эффективность терапии — это посмотреть на вирусную нагрузку. Неопределяемая вирусная нагрузка — верный признак того, что лечение работает как надо. С другой стороны, если лечение неэффективно, то вирусная нагрузка также покажет это:
- через несколько месяцев после начала новой схемы лечения вирусная нагрузка не снижается до неопределяемого уровня;
- неопределяемая вирусная нагрузка становится определяемой (обратите внимание: единичный «всплеск» вирусной нагрузки обычно не означает, что лечение неэффективно);
- определяемая вирусная нагрузка продолжает повышаться, несмотря на прием лекарств от ВИЧ в соответствии с прописанной схемой.
По показателям вирусной нагрузки можно понять, что терапия неэффективна, но нельзя понять почему. И вот здесь на помощь приходит тестирование на лекарственную устойчивость. Эти тесты помогут вам и вашему врачу определить, приобрел ли вирус устойчивость к лекарствам, которые вы принимаете, или, если вы еще не начали лечение, поможет выяснить, инфицированы ли вы лекарственно-устойчивым штаммом ВИЧ, и правильно подобрать лекарства.
Когда нужно сдать тест на резистентность?
Руководства по лечению ВИЧ, в США и странах Евросоюза, рекомендуют всем ВИЧ-положительным людям пройти тестирование на лекарственную устойчивость. Такое тестирование следует проводить в следующих случаях:
- При первичной постановке диагноза ВИЧ.Для подбора лечения полезно знать, инфицированы ли вы лекарственно-устойчивым штаммом ВИЧ и к каким именно лекарствам устойчив вирус в вашем организме. Для получения наиболее точных результатов тест на лекарственную устойчивость ВИЧ следует сдать вскоре после постановки диагноза, даже если в ближайшие несколько месяцев или лет вы не планируете начинать лечение (информация сохранится в медицинской карте и пригодится, когда начнется лечение). Однако важно отметить, что в таком случае тестирование на лекарственную устойчивость не всегда дает точные результаты. Как только лекарственно-устойчивый штамм попадает в организм, он начинает размножаться. Со временем может появиться штамм ВИЧ дикого типа, который вынудит лекарственно-устойчивые штаммы скрываться и становиться незаметным для тестов на лекарственную устойчивость. Другими словами, тестирование может дать ложные результаты, если с момента инфицирования прошло слишком много времени.
- Если лечение не помогает. Если вирусная нагрузка не достигает неопределяемого уровня после начала новой схемы лечения или снова становится определяемой, стоит провести тестирование на лекарственную устойчивость, чтобы определить причину происходящего. Для получения наиболее точных результатов тестирование следует проводить без прекращения лечения (если вирусная нагрузка определяемая) или в течение четырех недель после прекращения лечения. Если у вируса не обнаружена резистентность к лекарствам, то проблема может заключаться в недостаточно точном следовании схеме лечения (низкой приверженности), плохой абсорбции или лекарственном взаимодействии. Лучше всего решить эти проблемы до того, как разовьются мутации резистентности. Если обнаружена лекарственная устойчивость вируса, тестирование поможет определить, какие лекарства перестали работать в конкретном случае (у людей редко развивается устойчивость ко всем трем или четырем принимаемым препаратам), а также выяснить, на какие лекарства следует перейти.
- Во время беременности. Если ВИЧ-положительная женщина беременеет, то самый эффективный способ снизить риск передачи вируса ребенку — это достигнуть неопределяемой вирусной нагрузки и сохранять ее на этом уровне, по крайней мере, до рождения ребенка. Достичь этой важной цели также поможет тестирование на лекарственную устойчивость до и во время лечения.
Какие бывают тесты на лекарственную устойчивость?
В целом, существует два типа тестов на лекарственную устойчивость для ВИЧ-положительных людей: генотипический и фенотипический. Поскольку генотипическое тестирование дает результаты в течение одной-двух недель — а не двух-трех-четырех, как фенотипическое тестирование, — то люди, которые еще не начали лечение, обычно делают именно его. Людям, у которых терапия ВИЧ перестала работать, также рекомендуется прибегнуть к тестированию на резистентность, чтобы подтвердить неэффективность лечения и помочь подобрать новую схему. Если первая или вторая схема оказалась неэффективной, предпочтение отдается генотипическому тестированию. В руководстве говорится, что фенотипическое тестирование следует проводить при более обширной лекарственной устойчивости вируса.
Людям, которые уже принимали несколько препаратов в прошлом, лучше будет получить результаты обоих видов тестов. Одна компания, Monogram Biosciences, проводит фенотипирование и генотипирование образца крови и предоставляет результаты обоих тестов в одном лабораторном отчете под названием PhenoSense GT. В целом, оба теста дают наиболее точные результаты при вирусной нагрузке 500 и более, а лучше не менее 1000.
Что такое генотипическое тестирование?
Эти тесты проверяют текущую генетическую структуру — или генотип — ВИЧ, взятого у человека (для этого нужен только стандартный образец крови). ВИЧ исследуется на наличие определенных генетических мутаций, которые и вызывают устойчивость к тем или иным лекарствам.
Пример: ученым известно, что НИОТ «Эпивир» и «Эмтрива» не эффективны против форм ВИЧ, которые содержат мутацию «M184V» в гене обратной транскриптазы. Если генотипический тест на резистентность обнаруживает мутацию участка M184V, то велика вероятность, что ВИЧ человека имеет устойчивость к «Эпивиру» и «Эмтриве» и не поддается воздействию данных препаратов.
В отношении многих лекарств, в том числе ингибиторов протеазы и других НИОТ для возникновения резистентности требуются сложные комбинации мутаций. Таким образом, интерпретация результатов генотипического тестирования может представлять определенные сложности, поскольку разные мутации — и разные комбинации мутаций, особенно у ВИЧ-положительных людей с длительной и обширной историей лечения — могут означать разные вещи. Однако, поскольку за последние несколько лет наши знания о мутациях и их различных типах значительно расширились, лаборатории могут предоставлять врачам точную и полезную информацию.
В настоящее время можно сделать следующие генотипические анализы: HIV-1 TrueGene компании Bayer Health Diagnostics, ViroSeq от Celera Diagnostics/Abbott Laboratories, GenoSure (Plus) компании LabCorp и GeneSeq компании Monogram Biosciences.
Если вы хотите узнать больше об определенных мутациях и генотипировании, мы рекомендуем обратиться к сайту базы данных лекарственной устойчивости к ВИЧ Стэнфордского университета. Там приведены подробные списки различных мутаций, вызывающих устойчивость к каждому из одобренных антиретровирусных препаратов, а также специальный интерактивный инструмент, который можно использовать для перепроверки результатов генотипического тестирования.
Что такое фенотипическое тестирование на резистентность?
В отличие от генотипического тестирования, которое направлено на поиск определенных генетических мутаций, вызывающих лекарственную устойчивость, фенотипическое тестирование напрямую измеряет поведение — то есть фенотип — ВИЧ человека при воздействии определенных антиретровирусных препаратов. Из-за механизма фенотипических тестов и получаемых с их помощью результатов многие эксперты считают их более полными и надежными по сравнению с генотипическими тестами. Особенно это касается случаев, когда люди уже безуспешно пробовали принимать целый ряд различных препаратов от ВИЧ.
Говоря простым языком, фенотипическое тестирование проводится путем помещения образцов ВИЧ человека в пробирки с разными лекарствами от ВИЧ и наблюдения за реакцией вируса. Так оценивается способность вируса расти (или не расти) в присутствии того или иного лекарства. Вирус подвергается воздействию каждого лекарства в различной дозировке или концентрации. Способность вируса из организма конкретного человека расти в присутствии лекарств сравнивается с вирусом дикого типа, который на 100% чувствителен ко всем лекарствам против ВИЧ. Сравнение вируса из организма конкретного человека и вируса дикого типа и представляет собой результаты фенотипирования.
Эти результаты говорят врачам, какое количество конкретного препарата необходимо для сокращения репликации ВИЧ. Другими словами, лаборатория, проводящая фенотипический тест, пытается определить количество или концентрацию препарата, необходимого для предотвращения размножения ВИЧ.
Например, если для сдерживания репликации ВИЧ требуется в четыре раза больше НИОТ «Зиагена» (абакавира), то считается, что вирус обладает «четырехкратной устойчивостью» к препарату. Если требуется в семь раз больше «Зиагена», то вирус считается семикратно устойчивым к препарату.
Когда фенотипические тесты только появились, было трудно интерпретировать эти кратности резистентности. Было неясно, что означает кратность резистентности с точки зрения полной чувствительности вируса, его меньшей чувствительности или нечувствительности к конкретному препарату против ВИЧ. В результате компании, проводящие фенотипические тесты, начали тесно сотрудничать с исследователями, чтобы лучше понять кратность резистентности и то, что она на самом деле означает с точки зрения устойчивости вируса к имеющимся лекарствам. Результатом нескольких лет активных исследований стала разработка «клинических порогов». Этот важный элемент фенотипического тестирования значительно упрощает интерпретацию кратности резистентности, соотнося ее с чувствительностью ВИЧ к имеющимся лекарствам.
Возвращаясь к примеру с «Зиагеном», если мы возьмем анализ PhenoSense HIV от Monogram Bioscience, то нижний клинический порог соответствует 4,5-кратной резистентности, а верхний клинический порог соответствует 6,5-кратной резистентности. Другими словами, ВИЧ с четырехкратной устойчивостью к «Зиагену» в принципе еще чувствителен к препарату, тогда как ВИЧ с семикратной устойчивостью к «Зиагену» гораздо менее чувствителен к препарату и, следовательно, его не стоит включать в схему лечения.
Если показатель кратности резистентности находится между нижним и верхним порогами, то это означает частичную устойчивость (чем выше кратность резистентности, тем менее чувствителен ВИЧ к используемому лекарству). Конечно, лучше всего использовать антиретровирусные препараты, к которым вирус полностью чувствителен, но иногда приходится принимать (или повторно принимать) лекарства, к которым ВИЧ устойчив частично.
У всех лекарств от ВИЧ свои клинические пороги, и это иногда сбивает с толку. Чтобы помочь разобраться в этих пороговых значениях и облегчить медицинским работникам интерпретацию результатов, лаборатории, проводящие эти тесты, составляют подробные отчеты по каждому проведенному тесту.
Обычно используется один из двух «стандартных» фенотипических тестов: анализ PhenoSense компании Monogram Bioscience или Antivirogram компании Virco Lab. Оба теста оценивают кратность резистентности вируса в отношении всех имеющихся НИОТ, ингибиторов протеазы и ННИОТ. У Monogram Biosciences есть отдельный фенотипический анализ под названием PhenoSense Entry, который проверяет чувствительность ВИЧ к ингибитору проникновения «Фузеону».
Есть и другой тест — VircoTYPE HIV-1 от Virco Lab. Он, по сути дела, представляет собой «прогностический» фенотипический тест, использующий результаты генотипического тестирования для определения фенотипа вируса без фактического проведения фенотипического теста. Для этого в лаборатории проводится генотипическое тестирование и устанавливается, есть ли в образце ВИЧ мутации, вызывающие лекарственную устойчивость. После определения генотипа вируса лаборатория выполняет поиск в базе данных компании Virco, содержащей генотипы нескольких тысяч образцов ВИЧ, взятых у других людей. Затем она извлекает фенотипы — кратности резистентности, — которые соответствуют этим образцам, усредняет информацию и прогнозирует препараты, к которым текущий образец будет более или менее чувствителен.
Важно отметить, что Monogram Biosciences и Virco рассчитывают клинические пороговые значения по-разному. В результате пороговые значения, установленные для тестирования одной компании (например, PhenoSense), не применяются к пороговым значениям, установленным для анализа другой компании (например, vircoTYPE).
Вот как выглядит результат тестирования PhenoSense на лекарственную устойчивость:
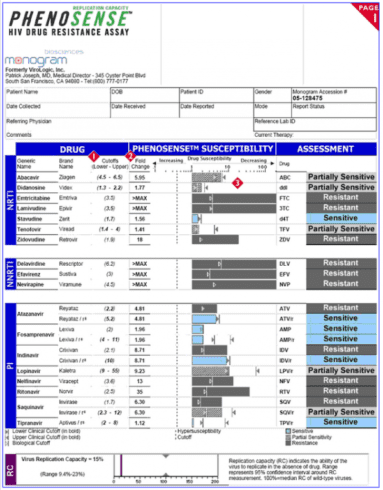
1) Пороговые значения
Жирным шрифтом выделены клинические пороговые значения; не выделенные жирным шрифтом числа — это биологические пороговые значения. Клинические пороги с двумя числами обозначают кратность резистентности (см. № 2), при которой действие лекарства на вирус начинает снижаться (первое число), и кратность резистентности, при которой препарат оказывает незначительное влияние на вирус или совсем не влияет на него (второе число).
2) Кратность резистентности
Чем выше устойчивость ВИЧ к лекарству, тем выше должна быть концентрация этого лекарства, чтобы предотвратить размножение вируса. Это увеличение концентрации и выражается в кратности резистентности. Чем выше кратность резистентости, тем меньше вероятность того, что препарат будет эффективен против ВИЧ.
3) Гистограмма кратности резистентности
Это графическое изображение кратности резистентности. Синие столбцы показывают, что кратность резистентности все-таки ниже концентрации препарата, необходимой для подавления ВИЧ; светло-серые полосы указывают на то, что кратность резистентности увеличена, но вирус все-таки хотя бы частично чувствителен к препарату; темно-серые полосы указывают на усиление кратности резистентности и низкую вероятность того, что вирус будет чувствителен к препарату.
Как избежать развития лекарственной устойчивости?
Чтобы предотвратить или хотя бы замедлить развитие резистентности, ВИЧ-положительные люди могут предпринимать следующие шаги:
- Узнать все, что можно, о лечении ВИЧ и имеющихся вариантах. Чем больше вы знаете, тем легче будет выбрать лечение, которое поможет избежать лекарственной устойчивости. Начать можно, например, с изучения информации о лекарствах от ВИЧ на этом сайте.
- Начинать терапию с сильнодействующей схемы лечения ВИЧ. Первая попытка лечения ВИЧ обычно является наилучшей возможностью для полного подавления вируса и предотвращения развития лекарственной устойчивости.
- При смене терапии новая схема должна быть наиболее эффективной. По возможности лучше переключиться на схему с тремя препаратами, которые, согласно результатам тестов на резистентность, будут эффективны против вируса. Если такой возможности нет, то два активных препарата лучше, чем один.
- Строго следовать указаниям врача. Очень важно принимать лекарства от ВИЧ в точном соответствии с предписаниями врача. Пропуск приема препаратов и нарушение режима дозирования способствуют росту вирусной нагрузки и развитию мутаций лекарственной устойчивости
- Общаться со своим врачом. Чтобы избежать развития лекарственной устойчивости, нужно точно знать, как правильно принимать лекарства, а также сообщать врачу обо всех возникающих проблемах.
- Следить за эффективностью терапии. То есть после начала лечения и до тех пор, пока вы принимаете препараты, обязательно следите за своей вирусной нагрузкой и результатами других анализов. Обычно рекомендуется сдавать анализы раз в три месяца. Возрастающая вирусная нагрузка — или неспособность достигнуть неопределяемой вирусной нагрузки — зачастую является первым признаком развития лекарственной устойчивости. Контроль вирусной нагрузки помогает вовремя принять меры и предотвратить развитие лекарственной устойчивости.